Face à un diagnostic de tumeur cérébrale, une question revient souvent : quelles sont mes chances et quels traitements existent vraiment ? Les réponses dépendent du type de tumeur, de son emplacement et de son profil moléculaire. Les chiffres sont utiles pour se repérer, mais ils ne résument pas une histoire individuelle. Avec les progrès récents, de plus en plus de patients gagnent en temps et en qualité de vie grâce à des prises en charge personnalisées.
💡 À retenir
- Les taux de survie à 5 ans varient en fonction du type de tumeur
- Les avancées dans les traitements augmentent les chances de survie
- Importance du suivi médical régulier pour les patients
Qu’est-ce qu’une tumeur au cerveau ?
Une tumeur cérébrale est une masse de cellules qui se multiplient de façon anormale à l’intérieur du crâne. Elle peut être primaire (née dans le cerveau) ou secondaire (métastase provenant d’un autre organe). Certaines sont dites bénignes, d’autres malignes, mais le terme « bénin » est relatif dans le cerveau, car l’emplacement peut compliquer la chirurgie et entraîner des symptômes importants.
La classification moderne ne repose plus seulement sur l’aspect au microscope. Elle intègre des critères moléculaires qui affinent le pronostic et guident les traitements. La classification de l’OMS 2021, mise à jour récemment, tient compte notamment des marqueurs IDH et 1p/19q pour les gliomes, et des altérations spécifiques pour d’autres entités. Ces précisions sont essentielles quand on parle de tumeur au cerveau chance de survie, car elles peuvent changer la trajectoire de soins.
Définition et classification des tumeurs cérébrales
On distingue les gliomes (astrocytomes, oligodendrogliomes et glioblastomes), les méningiomes, les neurinomes (schwannomes), les adénomes hypophysaires, les médulloblastomes, les épendymomes, ainsi que les métastases cérébrales. Les gliomes sont classés par grade selon l’agressivité et par biologie moléculaire, avec la mutation IDH et la co‑délétion 1p/19q comme déterminants majeurs. Les symptômes dépendent de la zone touchée : maux de tête persistants, crises d’épilepsie, troubles du langage, de la vision, de l’équilibre ou de la mémoire.
Chances de survie selon le type de tumeur
Les taux de survie s’expriment souvent à 5 ans. Ils varient largement selon le type de tumeur, l’âge, l’état général, l’accès à un centre expert et les marqueurs moléculaires. Les chiffres issus des registres (France, Europe, États‑Unis) donnent un ordre de grandeur à l’échelle de la population. Ils ne préjugent pas d’un parcours individuel, d’autant que les thérapies progressent.
Pour les patients et familles, parler de tumeur au cerveau chance de survie requiert nuance et contexte. Une tumeur de bas grade chez un adulte jeune avec marqueurs favorables n’a pas la même trajectoire qu’un glioblastome chez une personne âgée. Des progrès comme la chirurgie assistée, la radiothérapie de précision et la prise en compte du profil moléculaire améliorent la médiane de survie et la qualité de vie.
Statistiques sur la survie
- Glioblastome (adulte) : survie médiane autour de 12–18 mois avec prise en charge optimale, taux de survie à 5 ans souvent autour de 5–7 %.
- Oligodendrogliome IDH‑mutant, 1p/19q co‑délétion : temps de survie prolongé, taux à 5 ans fréquemment de 80–90 % selon les séries.
- Astrocytome IDH‑mutant (grade 2–3) : taux à 5 ans souvent entre 60–80 % selon l’âge, l’étendue de la résection et les traitements.
- Méningiome bénin (grade 1) : taux à 5 ans > 90 % après chirurgie et/ou radiothérapie adaptée.
- Médulloblastome (enfant) : taux à 5 ans autour de 70–85 % selon le sous‑groupe moléculaire et le protocole.
- Adénome hypophysaire : espérance de vie proche de la normale, contrôle tumoral durable dans la majorité des cas.
- Métastases cérébrales : très variable selon le cancer d’origine, le nombre de lésions et les thérapies ciblées ; survie médiane de quelques mois à plus d’un an dans des situations sélectionnées.
Ces chiffres évoluent grâce aux thérapies combinées, aux nouvelles molécules et à une meilleure sélection des patients. Les essais récents montrent des bénéfices spécifiques pour certains sous‑groupes, par exemple en cas de méthylation de MGMT ou d’altérations ciblables.
Traitements disponibles pour les tumeurs cérébrales
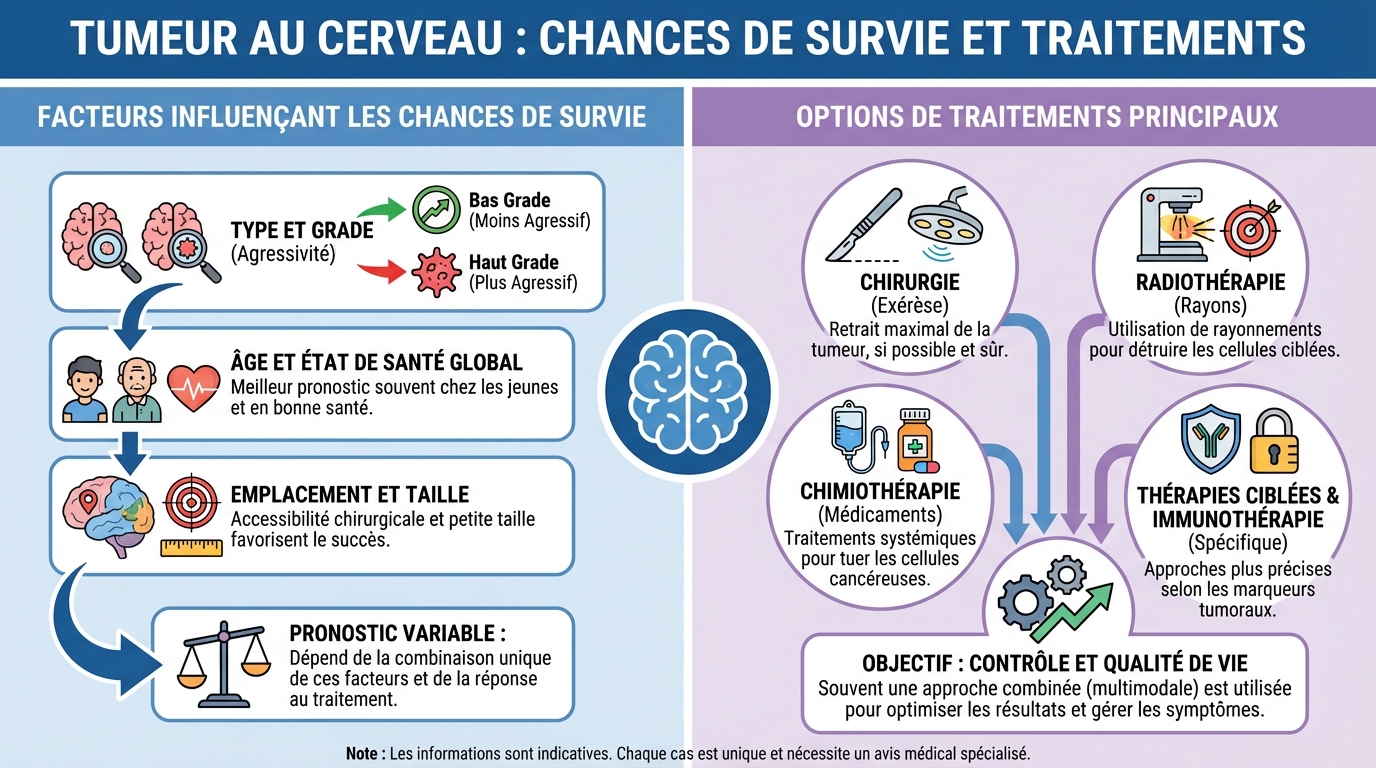
La prise en charge est pluridisciplinaire : neurochirurgien, radiothérapeute, oncologue, neuroradiologue, neuropathologiste, neuro‑oncologue, rééducateurs. Les décisions se font en réunion de concertation pluridisciplinaire, au cas par cas, en fonction de la localisation, de la taille, de l’accessibilité chirurgicale et des marqueurs moléculaires. Les plans de traitement visent à maximiser le contrôle tumoral tout en préservant les fonctions neurologiques.
Le profil moléculaire guide de plus en plus les choix. Par exemple, un gliome IDH‑mutant peut bénéficier de schémas de chimiothérapie prolongés, tandis que la méthylation du gène MGMT prédit une meilleure réponse au témozolomide. Ces nuances comptent lorsqu’on parle de tumeur au cerveau chance de survie, car elles orientent les stratégies les plus efficaces pour chaque patient.
Chirurgie, radiothérapie et chimiothérapie
- Chirurgie : viser une résection maximale sans séquelles. Techniques d’éveil, cartographie fonctionnelle, fluorescence (5‑ALA) et neuronavigation améliorent la sécurité. Effets possibles : troubles transitoires, fatigue, crises d’épilepsie, infections rares.
- Radiothérapie : conformationnelle, stéréotaxique, voire protonthérapie selon l’indication. Effets fréquents : asthénie, irritation cutanée, œdème cérébral temporisé par corticoïdes. Effets différés : troubles cognitifs potentiels, surveillés en consultation dédiée.
- Chimiothérapie : agents alkylants dont le témozolomide, schéma Stupp pour glioblastome, PCV pour oligodendrogliome. Effets : nausées, baisse transitoire des globules, alopécie variable, nécessitant une surveillance hématologique.
D’autres options complètent l’arsenal : inhibiteurs anti‑angiogéniques, thérapies ciblées selon altérations, champs électriques tumoraux (TTFields) dans certaines indications, essais d’immunothérapie. La rééducation (orthophonie, kinésithérapie, neuropsychologie), la prise en charge de l’épilepsie et le sevrage progressif des corticoïdes améliorent la qualité de vie.
Témoignage court : « Karim, 52 ans, a bénéficié d’une chirurgie suivie de radio‑chimiothérapie. Les réunions régulières avec son équipe lui ont permis d’ajuster traitements et rééducation. Il a repris une activité partielle, avec des objectifs réalistes et des pauses planifiées. » Ce type d’accompagnement structuré compte autant que la technique pour la tumeur au cerveau chance de survie.
Facteurs influençant les chances de survie
Plusieurs paramètres modulent le pronostic : l’âge, l’état général, le type et le grade de la tumeur, son profil génétique, l’étendue de l’ablation chirurgicale et la réponse aux traitements. L’accès rapide à un centre expert et à des essais cliniques peut offrir des options supplémentaires.
La biologie de la tumeur est centrale. Certains marqueurs sont associés à des trajectoires plus favorables, d’autres à des formes plus agressives. La personnalisation des soins s’appuie sur ces informations pour améliorer la tumeur au cerveau chance de survie à l’échelle individuelle.
Âge, santé globale et type de tumeur
- Âge et état fonctionnel : un meilleur score de performance (KPS) permet des traitements plus intensifs et une meilleure tolérance.
- Étendue de la chirurgie : une résection complète quand elle est possible est corrélée à une survie prolongée, tout en respectant les zones éloquentes.
- Profil moléculaire : mutation IDH, co‑délétion 1p/19q et méthylation MGMT sont liés à une meilleure réponse à la chimiothérapie et au pronostic.
- Localisation : les tumeurs profondes ou proches des aires du langage/moteur limitent parfois l’exérèse complète et nécessitent des approches combinées.
- Accès au suivi spécialisé : IRM régulières, réadaptation, gestion des effets secondaires et inclusion précoce en essai clinique quand cela est pertinent.
Conseils pratiques : demander une relecture anatomopathologique avec profil moléculaire complet, solliciter un deuxième avis en centre expert, préparer une liste de questions avant chaque rendez‑vous, et noter les symptômes entre les consultations pour guider les ajustements de traitement.
Vivre avec une tumeur au cerveau
Le parcours s’inscrit dans la durée, avec un calendrier de contrôles, de rééducation et d’adaptations au quotidien. Les consultations de suivi neuro‑oncologique s’accompagnent d’IRM régulières, souvent IRM tous les 3 à 6 mois au début, puis espacées selon la stabilité. L’objectif est d’anticiper, de traiter précocement les rechutes et de préserver l’autonomie.
Les soins de support font la différence : prise en charge de la fatigue, de la douleur, de l’humeur, de la cognition, de la nutrition et du sommeil. Un carnet de bord des symptômes aide à objectiver les variations (maux de tête, crises, troubles de concentration). Exemple concret : planifier les activités demandant de la concentration le matin, prévoir des pauses de 15 minutes toutes les 90 minutes, et protéger le sommeil avec une routine stricte.







